太田教授谈氢医学发现历史
氢医学的创立、进展和今后可能发展
太田成男
生化学 第87 卷第1 号,pp. 82‒90(2015)
氢分子一直以来都被认为是惰性的,在哺乳类细胞内无法发挥作用的分子。笔者证明,氢气在细胞中能够消除羟基(·OH)这样的氧化力强的物质,改变了以往观念,并提出氢气可能应用于疾病预防和改善。氢在组织和细胞中扩散迅速,不会破坏氧化还原反应系统,也不会扰乱活性氧物质信号传递功能。氢也能通过影响基因表达启动体内自身抗氧化作用,还有抗炎作用、抗过敏作用、抗细胞凋亡作用和促进能量代谢等广泛功能。通过实验动物模型所获得的证据在不断积累,而且也进行了许多临床试验,更多研究仍在进行中。一般传统药物只对特定靶向目标发挥特异作用,氢气不同于大部分传统药物,能对多种目标产生效应,因此,氢具有不同于传统药物的特点。
1. 序言
氢分子是化学式为H2的所谓氢气,也被称为分子氢,在本文只简称氢。一直以来,在哺乳动物细胞内氢被认为不具有活性。实际上,在体温条件下,氢如果没有催化剂,不会和含氧化合物发生反应。在拥有氢化酶的许多细菌中,氢在酶促作用下分解,可被作为能源使用。或者也可能变成无氧代谢的产物。(点评:细菌能消耗氢气,也能制造氢气,这里只重点描述了利用氢气)。
哺乳类动物没有氢化酶基因,氢气在体温条件下相对稳定,所以人们推测氢在哺乳类体内是不发挥作用的。2007年,笔者们通过一篇论文证明,H2能消除细胞中的羟基自由基(·OH)和过氧亚硝酸阴离子(ONOO-)等氧化力很强的活性氧和活性氮,对抗氧化应激,具有细胞保护作用,从而改变了传统观念。从那以后,许多人使用模型动物对氢的改善和预防效果进行研究,已经发表了超过350篇论文。这些论文证明,在几乎所有器官中,无论是直接还是间接,氢对氧化应激有关模型疾病都有效果。并发现氢具有许多功能,例如抗炎、抗细胞凋亡和抗过敏作用,还有活化能量代谢作用。除了模型动物实验的论文之外,迄今已发表了超过10篇的临床试验论文。不仅在医学上,在农业中的应用也进入人们视野,有多篇证明氢对植物有效的论文。
本文回顾了氢生物学效应的发现经过,并对其效果和分子机制进行考察。
2.氧化应激的病理和生理作用
1)氧化应激病理作用
作为氧化性磷酸化能量代谢的副产品,好氧生物会日常性在其体内产生活性氧(活性氧)。此外,受吸烟、大气污染、紫外线、辐照、激烈运动、躯体或心理应激等因素影响,产生过量活性氧。当活性氧过量产生而内源性抗氧化能力减弱时,就会发生过氧化引起有害作用,从而形成“氧化应激”。炎症、心肌梗塞、脑梗塞、器官移植以及手术止血时缺血再灌注等状况都会产生急性氧化应激(6,7)。许多研究表明,慢性氧化应激与癌症、糖尿病、动脉硬化、慢性炎症性疾病以及大多数神经退行性疾病等病理状态和衰老都有关系(8)。
2)活性氧的生成过程
作为活性氧生成的第一步,是先产生超氧阴离子自由基(O2-)。这些超氧阴离子自由基大多数是因为线粒体电子传导系统的电子泄漏产生,所以经常说线粒体是活性氧的源头。此外,其他蛋白酶如NADPH氧化酶、细胞色素P450、脂氧合酶、环加氧酶和黄嘌呤氧化酶也分别与免疫系统和解毒系统产生活性氧有关9)。
在超氧化物歧化酶(SOD)催化作用下,超氧阴离子自由基转化为过氧化氢(H2O2),进一步被过氧化氢酶催化反应后形成水(H2O)。存在具有催化作用的过渡金属离子如Fe2+离子或Cu+离子情况下,通过Fenton反应或Weiss反应,过氧化氢或超氧阴离子自由基转变成高反应性的·OH 10)。氧阴离子自由基与一氧化氮(·NO)反应就会产生ONOO-这种高活性的活性氮物质(RNS)11),它与·OH一起成为氧化和破坏生物分子的主要原因12)。宇宙射线等放射线也可以电离水分子产生·OH。
3)过氧化氢的生理作用
如上所述,活性氧通常一直被认为只会引起细胞损伤并对生物体有害。然而,细胞氧化还原稳态处于活性氧产生和抗氧化系统之间的微妙平衡中13)。现在已知几种活性氧是作为调节多种生理机能的信号传导分子来发挥作用14,15)。
此外,由过氧化氢和·NO引起的氧化应激会诱导与抗氧化和抗性有关的酶,保护细胞免受氧化应激损伤16,17)。例如,转录因子NF-E2相关因子2(Nrf2)转移到细胞核中就会启动抗氧化基因表达,这些基因能防御重金属等有毒物质的毒性18)。过氧化氢也是细胞分化19)、免疫系统20)、自噬21)和细胞凋亡22)的重要调节因子,是维持细胞内稳态不可缺少的成员。因此,为维持细胞正常功能,绝对不能彻底消除过氧化氢。
4)理想的抗氧化剂
氧化损伤引起各种疾病,人们虽然期待这些疾病可通过抗氧化剂来改善和预防,但过去一直没有取得成功23)。所谓抗氧化补充剂已被证明在预防癌症、心肌梗塞和动脉粥样硬化方面基本无效,相反长期大量使用这些抗氧化剂还会增加死亡率23-26)。因此,在开发有效的抗氧化剂以预防与氧化应激相关疾病时,对消除活性氧时带来的副作用也是非常重要的。
考虑到这些情况,理想抗氧化分子应该是能缓解过多氧化应激,但又不能过多影响氧化还原稳态。换句话说,理想的抗氧化分子不应该过度减少过氧化氢这样的功能信号分子,但又必须能针对性有效减少像·OH这样的强氧化剂。考虑到这些因素,作者基于实验结果得出结论,氢就是理想的抗氧化分子。
3.发现氢分子的生物学效应
在探索理想的抗氧化分子过程中,我们进行了以下实验。通过施用线粒体电子传递链抑制剂抗霉素A,使培养PC12细胞暴露于氧化应激中,这些细胞对氧化应激作出反应,显示出异常形态改变。在不改变pH、氧气和二氧化碳浓度等条件下,将氢注入培养皿,即使施加相同氧化应力,细胞也不再显示形态改变。当从培养液中除去氢后,细胞就再次对氧化应激作出反应,发生形态改变。这些结果表明,氢直接作用于细胞发挥抗氧化作用,且氢气没有通过影响培养液成分发挥作用(除去失效)。基于第一次实验获得的这些结果,我们开始认为氢具有很大的实际临床应用潜力,并开始大力研究氢,那是2005年1月的事情。
接下来,我们尝试确定氢在培养细胞中起作用的分子标靶。即使把氢气溶解到培养液中,检测超氧阴离子自由基的荧光染料MitoSOX和检测过氧化氢的荧光染料DCF-DA(dichlorofluorescein diacetate)的荧光信号在细胞中没有出现变化。此外,采用DAF-2DA(diaminofluorescein-2 diacetate)来检测由DAF-2 DA(S-nit活性氧o-N-acetyl-D,L-penicillamine)诱导的·NO的细胞内水平时,发现到·NO也不会被氢气消除。与此相对照地,在施用氢时,·OH的检测用荧光染料HPF(hydroxyphenylfluorescein)27)的荧光信号却降低了(图1)。随后再通过电子自旋共振(ESR)自旋捕获方法证实氢降低细胞内·OH水平。
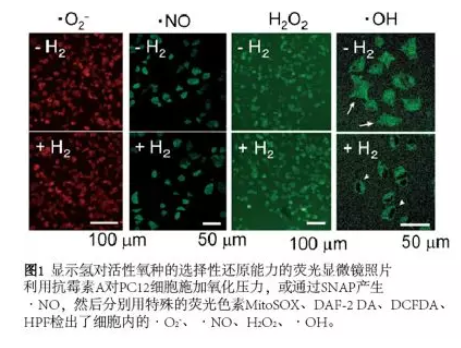
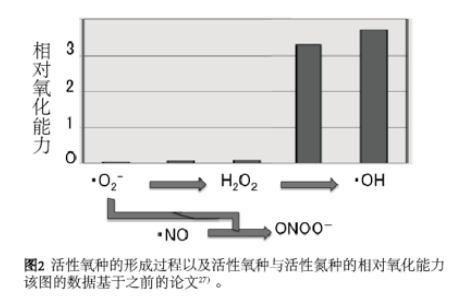
氢与活性氧的选择性反应可以通过·OH的氧化能力非常强大这点来解释,如图2所示。这意味着·OH具有足够强氧化能力能与惰性的氢发生反应,而超氧阴离子、过氧化氢和一氧化氮自由基没有能与氢反应那么强的氧化能力。换句话说,氢的作用温和,不影响代谢氧化还原反应,也不影响具有细胞内信号传导功能的活性氧。氢具有选择性抗氧化作用。
4.氢与其他医学气体比较
在此,让我们与其他医学气体进行比较。硫化氢(H2S)和一氧化碳(CO)、一氧化氮(·NO)都是毒性很强的分子,但它们作为信号转导分子却发挥重要作用28-30)。最近研究表明,血红素蛋白作为这些气体分子靶标起着重要作用。线粒体细胞色素c氧化酶也是一种血红素蛋白,在线粒体呼吸链中发挥核心作用30)。然而,由于氢不与血红素反应,因此氢的主要目标应该与其他医学气体不同。细胞通过·NO合酶、胱硫醚γ-裂解酶、胱硫醚β-合酶和血红素加氧酶(HO-1)的酶促反应,能分别合成·NO、H2S、CO30,31)。相反,如上所述,哺乳动物不具有能在其细胞中产生氢的酶。
与其他医学气体相比,氢具有完全无细胞毒性的优点。已经在人体中证实,即使在高氢浓度下也没有细胞毒性32,33)。
并且,氢气容易燃烧,只需要高于527℃温度就可点燃,但空气中氢气仅在爆炸范围(4~75%,体积比)浓度下,才可能会与分子氧反应而发生爆炸。如后所述,由于吸入1%~4%浓度的H2气体就非常有效,因此氢气应该能在临床上广泛使用,而无需担心爆炸危险2,34)。
5.氢气的摄取方法
1)氢气吸入
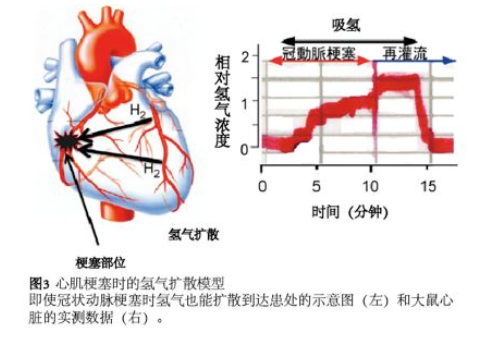
吸氢是将氢气摄入体内的最简单方法。由于吸入氢气能迅速被肺吸收,然后通过血液循环短时间内运输到全身,因此吸入氢气适合用于防止急性氧化应激。特别是心肌梗塞,若采取静脉点滴氢气溶液注射,因增加血容量会导致血压升高,在心肌改善中加重损伤,但氢气吸入则不影响血压2)。通过实验证实,氢气甚至可以扩散到血管已经梗塞、血流已经停止的梗死组织内,能防止缺血再灌注时活性氧的伤害,这点也是它不同于其他药物的一个优势(图3)。
在动物实验中,吸入约1%~4%氢气确认有效,在临床试验中,给病人吸入3~4%氢气安全性和血液氢浓度变化也已经确认35)。对人的脑缺血和心肌缺血改善效果也有了小规模临床证据(2017年)。
2)饮用氢水口服摄入
考虑到氢气吸入比较不方便,为了预防疾病日常使用氢气,比较方便的方法是饮用氢水。氢水可以随身携带,单靠喝水就能摄取氢气,更安全且实用36,37)。在室温大气压下,氢在水中最大可溶解至0.8mM(1.6mg/L),不改变水的pH值。饱和氢水比稀释氢水更有效,但研究发现稀释10倍的80μM的氢水也能有效改善小鼠肥胖症38)。研究结果表明氢气的有效剂量比原来想象的更低,效果可能超过预期。氢气分子体积非常小,一般的塑料包装材料无法长时间维持氢水浓度,采用金属容器才能长时间保持氢气不泄漏。
3)含氢生理盐水注射
将氢气溶解到生理盐水中,以含氢生理盐水形式进行静脉或腹腔注射,这种方法已在实验动物中高效地提供氢气39),这种方法的安全性已在临床试验中得到验证40)。
4)局部使用氢:滴眼液、沐浴、化妆品
利用氢的强大扩散性,能经体表吸收到体内。研究证实,溶解氢气的滴眼液直接施用于眼球表面,氢气会扩散到没有血流的眼球当中41,42)。低温保存心脏移植物放入氢水浸泡,利用扩散性供氢气,可有效缓解心肌再灌注损伤43)。
氢气容易穿过皮肤,通过血液运输到全身。氢气热水沐浴是日常生活中摄入氢气的理想方式,已有几家公司在市面销售氢水浴沐液。
6.氢的检测和体内动态变化
氢作为抗氧化剂有效的原因还在于其物理性质,因为氢分子量很小,能迅速穿过生物膜并扩散到细胞液中,并很快到达细胞核和线粒体,可保护核和线粒体DNA2)。氢还能自由穿过血脑屏障,这对大脑和脊髓疾病改善是非常有价值。
氢气的溶解度比较小,生物组织和水中含有大量氢原子,采用气相色谱无法对液相内氢气浓度进行直接测量。将血液或器官内氢可释放到气相,然后通过气相色谱法测量可以显著提高测试灵敏度。给大鼠吸入氢气后,动脉血中氢浓度随吸氢浓度增加而增加,静脉血氢水平低于动脉血中。动脉和静脉血之间浓度差提示氢气被组织摄取和消耗掉氢气量2)。小鼠喝饱和氢水后数分钟内血液中检测到微摩尔级氢气37,44)。
组织中氢浓度动态改变可以通过氢电极即氢传感器分析。例如在大鼠心肌中,电极插入梗塞部位测量氢气,结果发现即使在冠状动脉完全闭塞血流完全中断,氢气在缺血组织内也会升高,提示氢气能从未缺血组织扩散到缺血组织34)(图3)。将氢气滴眼液直接滴到大鼠角膜上,通过角膜将针状氢传感器电极插入玻璃体并进行连续监测,证明氢气能跨过角膜扩散到玻璃体41)。此外有研究用针型氢传感器监测肝脏组织氢气,测量肝组织内氢气动态改变38)。
通过气相色谱法测量成人受试者饮用氢水后呼气中氢含量,当摄取氢水后,呼气中氢含量迅速上升,摄取后10分钟到达峰值,在60分钟内返回基线。饮用氢水内氢气大约有40%在体内被利用,表明摄入氢气至少有一部分是被·OH等氧自由基清除捕捉到了45)。
7.氢分子的效果和临床试验
1)对缺血再灌注损伤的保护作用
缺血再灌注会产生大量的活性氧并损伤组织。给动物吸入氢气后,改善了脑梗塞2)和心肌梗塞34)期间的缺血再灌注损伤(图4)。腹腔注射氢气生理盐水,保护肾脏免受缺血再灌注损伤46)。心肺停止后复苏后障碍源于大脑和心脏等器官缺血再灌注损伤。通过吸入氢气,大鼠心脏骤停后存活率和神经病变都得到很大改善47)。

无论是吸氢气48)、喝氢水49),或把器官浸入含氢液43),都能减少器官移植后损伤。事实证明,不管何种方法,只要有氢气摄入,就可以产生效果。用氦气对照,就没有这种作用,这说明氢气是产生作用的根源,氢气的还原性是产生作用的条件50)。
2)对神经变性的作用
慢性氧化应激被认为是神经退行性疾病如痴呆和帕金森病的原因之一51)。通过施加慢性束缚应激,可诱导大脑氧化应激,造成学习和记忆障碍52)。受束缚应激影响,海马齿状回神经细胞增殖会受到抑制。通过饮用氢水,这一氧化应激过度得到抑制,且预防了学习、记忆和空间认知机能的功能障碍。在实验动物模型中,氢水促进了海马齿状回神经细胞增殖37)。考虑到抗抑郁药被认为可增加成人神经元新生53),所以氢水可能对改善抑郁症等精神障碍也是有效的。
在帕金森病中,与线粒体功能障碍相关的氧化应激被认为是黑质多巴胺能神经元丢失的主要原因54)。利用羟基多巴胺(6-OHDA)的毒性造成黑质纹状体变性的帕金森氏病大鼠模型,在6-OHDA给药前或给药后给动物们饮用氢水,发现大鼠黑质纹状体变性的形成和发展都被阻止55)。此外,利用1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine(MPTP) 诱导的另一种小鼠帕金森病模型中,多巴胺能神经元丧失也能被氢水饮用抑制56)。
基于这些显著结果,实施的一项随机双盲临床试验,让帕金森病患者饮用氢水48周,根据临床帕金森病评价指标(Unified Parkinson’s DiseaseRating Scale,UPDRS)进行判断,结果显示氢水具有显著改善人类帕金森病的效果57)。
3)促进能量代谢和改善代谢综合征的作用
饮用氢水后,能量代谢被激活38)。氢水显著改善肥胖的2型糖尿病模型小鼠db/db小鼠脂肪肝症状。虽然食物和水摄入量完全相同,但长期喝氢水却显著减少体脂肪和体重(不少吃饭,体重下降,是不是让许多胖妹纸激动)。此外,发现喝氢水后氧气消耗量和二氧化碳排放量增加,这表明通过活化能量代谢而降低了血浆葡萄糖水平和胰岛素、甘油三酯水平38)。此外,给动脉硬化模型小鼠持续饮用氢水后,动脉硬化得到抑制36)(图5)。

中国山东泰山医学院一个研究小组在给代谢综合征受试者饮用氢水10周后,发现总胆固醇(TC)和LDL胆固醇水平降低了。并且,氢水抑制了氧化LDL、肿瘤坏死因子α(TNF-α)诱导的单核细胞与内皮细胞粘附,显著改善了胆固醇从巨噬细胞泡沫细胞中外流活性等58)。
总之,这些结果强烈暗示,患有代谢综合征的患者是可以期待氢水的饮用效果的。
4)对运动疲劳和损伤的影响
使用交叉双盲法以年轻男子足球运动员为测试对象,研究了氢水对运动的影响。结果发现,服用安慰剂水的受试者,在剧烈运动后血液乳酸水平升高了,但喝氢水时,剧烈运动期间血液乳酸水平上升得到了抑制,肌肉疲劳也得到缓解59)。
5)抑制炎症的作用
利用刀豆蛋白A、葡聚糖硫酸钠、脂多糖(LPS)、酵母聚糖(诱发全身广泛性炎症的物质)、严重细菌感染引起的脓毒症等炎症动物模型中,饮用氢水、注射氢气生理盐水、吸氢都能降低炎性细胞因子水平,并抑制炎症损伤5)。
针对类风湿性关节炎等慢性炎性疾病,双盲对照临床试验也证实饮用氢水具有改善效果60)。
6)减轻癌症改善副作用
吸入氢气和饮用氢水改善了小鼠抗癌药物顺铂改善所引起的体重减轻,改善肾毒性,降低死亡率。尽管对顺铂毒性具有保护作用,但氢却不影响顺铂对体外癌细胞系和体内肿瘤小鼠的抗肿瘤作用44)。
针对接受恶性肝肿瘤放射改善患者进行的6周摄取氢水双盲试验结果显示,血清抗氧化能力得到维持,生活质量(QOL)评分得到提高61)。
7)对其他疾病模型及患者的影响
已经证明摄取氢气在很多种疾病模型中都有效,包括耳聋、角膜障碍、牙周病、非酒精性肝炎、高血压、骨质疏松症、解毒等,作用非常广泛5)。

临床试验中,除上述情况外,还有对皮肌炎和线粒体疾病的改善效果、对血液透析副作用的缓和效果,对急性红斑性皮炎和间质性膀胱炎患者用氢气也取得了理想效果5)。据闻某些自由诊疗诊所在积极使用氢气,并收到良好临床改善效果。
上述动物实验和临床试验的结果总结在图6中。氢气咋看上去在完全不同类型的疾病组中也是有效的。
8.氢分子作用的分子机制
如上所述,大量实验都证明氢具有广泛功能。在双盲临床试验中也被证明有效。然而,很难说这些功能的分子机制已经被解明。我想从直接和间接作用两方面对这个问题进行探讨。
1)氢分子直接中和羟基自由基
使用培养细胞的实验中,氢还原·OH是通过荧光试剂反应和自旋探针俘获法确认的2)。之后,证明氢滴眼药直接减少利用视网膜缺血再灌注所诱发的·OH 41),中国学者也在组织水平显示,氢气能中和利用放射线在精巢诱导的·OH 62)。
众所周知,·OH是自由基连锁反应的启动者。在生物膜上一旦产生这种自由基连锁反应,反应就会持续扩大,最终对细胞造成严重损伤。一旦发生自由基连锁反应,过氧化脂质就会增加,变成引起各种疾病原因之一。脂质过氧化会产生4-hydroxyl-2-nonenal(4-HNE)和丙二醛(MDA)等氧化应激反应标记物63),很多研究都表明,氢气能降低这些氧化损伤标记物。
因此,这些观察结果暗示,只要存在足够量氢气,那么被·OH诱发的组织氧化就可能得到有效缓解。但是,通过饮用氢水等方式,体内氢浓度不够高的情况下,这种解释就很难让人信服。(氢气作用太强,剂量小作用很大,无法让人容易接受)
2)氢分子直接还原过氧亚硝酸盐对基因表达进行调节
作为另一种分子机制,有必要考虑氢气对ONOO-的消除。已知ONOO-能修饰蛋白酪氨酸以产生硝基酪氨酸11)。无论是氢水49)、氢气64)还是氢生理盐水65),通过摄取氢气显示出有效地降低了实验动物模型中的硝基酪氨酸水平,人饮用氢水后,类风湿性关节炎患者的硝基酪氨酸水平也下降了60)。因此,氢的作用至少一部分可能是由于蛋白质硝基酰化受到了抑制。
由于已知许多参与转录控制的蛋白质因子被硝化(-O-NO2)或亚硝化(-S-NO2),因此认为,只要减少-O-NO2或-S-NO2,各种各样的基因表达就能得到控制11)。
3)控制信号转导
氢能阻碍ASK1及其下游信号分子p38 MAP激酶和JNK、IκB的磷酸化,调节信号传导66)。而且,氢还被证明可以抑制包括MEK、p38和ERK-1/2在内的多个信号蛋白的磷酸化49),并且也有报告指出氢能使NF-κB失活67)。这些研究都在暗示氢气能影响信号转导并调节基因表达。至于它是通过什么机制参予信号传导系统,目前正在详细分析。
4)通过调节基因表达间接地减少氧化应激
氢能诱导HO-1和SOD、过氧化氢酶和髓过氧化物酶等抗氧化系统,减轻氧化应激5)。
已知Nrf2通过诱导包括HO-1在内的多种基因而起到抵抗氧化应激和各种毒物的防御作用。Nrf2缺损小鼠即使吸入氢气也不会改善与HO-1减少相关的过氧化性肺损伤,似乎氢气依赖于Nrf2来参与过氧化性肺损伤的改善68)。
5)调节炎性细胞因子和荷尔蒙的基因表达
在大多数炎症模型中,氢气都是通过减少炎性细胞因子的表达来发挥抗炎作用3-5)。这种炎性细胞因子等增强炎症的能被氢气抑制其表达的因子有,TNF-α、白细胞介素(IL)-1β、IL-6、IL-10、IL-12、CCL2、干扰素(INF)-γ、细胞间粘附分子1(ICAM-1)、PGE1和PGE2、high mobility group box 1(HMGB-1)等3-5)。
如前所述,氢水能改善肥胖和代谢参数。分析基因表达的结果表明,饮用氢水可增加肝荷尔蒙的成纤维细胞生长因子21(FGF21)的表达。FGF21具有激活脂肪酸和葡萄糖消耗的功能38)。
饮用氢水后,生长素(ghrelin,一种促进分泌生长素的物质)在胃中的表达增加了。由于氢水的神经保护作用在施用生长素受体拮抗剂后消失了,因此这暗示与ghrelin是有关的69)。
6)调节其他基因表达
氢针对多种多样的病理状态在增加抗凋亡因子这一方向上进行调节,并且同时在减少促凋亡因子的方向上进行调节,从而在抑制细胞凋亡的方向上发挥作用。事实上,氢激活了Bcl-2和BclxL的抗凋亡因子的表达,并抑制了caspase 3、caspase 8和caspase12等促凋亡因子的表达。氢不仅降低了促凋亡性的Bax(Bcl-2-associatedX protein)的基因表达,还抑制了Bax的活化即向线粒体的移动70)。
氢似乎在改善各种病理状况的方向上调节基因表达。氢调节基因表达极具多样性,诸如MMP2/MMP9、MMP3/MMP13、脑利尿肽、ICAM-1/髓过氧化物酶、环氧合酶2(COX-2)、一氧化氮合酶(nNOS和iNOS)、连接蛋白30/43、胶原蛋白III、钙结合蛋白1(Iba1)等3-5)。
这些分子并不是氢的主要响应者,可能是通过间接作用使氢的各种作用得以发挥出来。
7)氢作用机理中的问题
许多实验和临床试验证实了氢的生物学和医学作用。但是,为了阐明分子机理,有必要考虑以下问题:
氢是一种惰性分子,可以在没有催化剂的情况下反应的分子应限于具有很强氧化能力的分子,如·OH和ONOO-。
水溶液中氢和·OH的反应速率比·OH和谷胱甘肽等还原性物质慢1000倍71)。水溶液中的低浓度氢,不可能通过与细胞中存在的谷胱甘肽等的竞争反应来消除·OH。
氢没能还原氧化型的辅酶NAD+和FADH,即使在存在酶的情况下也没能向NADH和FADH2转换(未发表)。
氢不能还原过渡金属。通过2Cu2++ H2→2Cu++ 2H+反应进行还原时,应可以在pH下灵敏检测得到。例如在pH7时,可以显著检测到的0.01ΔpH,也应该可以检测到10-9的数量级,但通过pH的变化则没有检测到氢的还原性。此外,血红素铁也没能还原(未发表)。
由于线粒体内膜的细胞质侧带正电并且具有非常高的电压,因此曾想象可能有H2→H+ + H-(假设H-被线粒体的正电荷吸收)这样的反应,但没有检测到。
为了证明氢的反应性,需要铂金属或铜金属等催化剂,但不认为这种催化剂在细胞中大量存在。此外,从细胞提取液中没有确认到任何催化与氢反应的活性。
氢分子很小,所以不可能存在可以特异性结合氢的受体。因为蛋白质的振动大于氢的大小,所以它们不能固定氢。在许多情况下,蛋白质与低分子要牢固结合必须固定在三个点上,但它无法3点固定氢分子。
与大肠杆菌和威尔士真菌这些肠内细菌能产生大量氢气相比,通过饮用氢水所摄取的氢气量非常小。但是,在信号传导的调节上,氢浓度的变化要比氢含量更为重要72)。
以上讨论是基于水溶液中的反应这个前提。例如,许多酶反应在实验中通常需要几分钟以上的时间来测量反应速率,但许多生物体内的反应是以毫秒量级进行的。因此,在生物体内,稀释水溶液中的反应速率是不适用的。细胞内通过复杂的生物膜和粘性溶液被高度地组织在一起,并且许多组分浓缩地存在着。由于碰撞频率是粘性环境中的速率控制步骤,因此氢的扩散速率快可能变成克服低反应速率常数的一项优点。而且,氢也可能局部存在于某些特定场所。
作者最近确定了氢调节信号转导和基因表达的首要标靶,可能在不久的将来就能对这些问题作出解答(投稿中)。
9. 结语
最近,氢气对植物的影响已陆续报道,主要是对盐害、根系发育和水果保鲜的效果。氢不仅只在医疗上,还可能对农业产生重大影响73,74)。
本文概述了氢气医学从黎明破晓到临床应用的发展过程。与氧化应激和炎症相关的氢气,对几乎所有的病理状态都有很大的效果。而且,氢没有有害的副作用,可以相对容易地进行验证和应用。事实上,它已经显示出对超过10种以上的疾病具有积极正面的临床效果。大多数药物只专门针对各自的靶标,所以在考虑氢的效应时,有必要引入全新的概念。氢对广泛多样的疾病有效,因此能应用到很多疾病的预防和改善中的可能性很大。
文献
1) Fritsch, J., Lenz, O., & Friedrich, B. (2013) Nat. Rev. Microbiol.,11, 106‒114.
2) Ohsawa, I., Ishikawa, M., Takahashi, K., Watanabe, M.,Nishimaki,K., Yamagata, K., Katsura, K., Katayama, Y., Asoh, S., &Ohta, S.(2007) Nat. Med., 13, 688‒694.
3) Ohta, S. (2011) Curr. Pharm. Des., 17, 2241‒2252.
4) Ohta, S. (2012) Biochim. Biophys. Acta, 1820, 586‒594.
5) Ohta, S. (2014) Pharmacol. Ther., 144, 1‒11.
6) Ferrari, R., Ceconi, C., Curello, S., Cargnoni, A.,Pasini, E., & Visioli,O. (1991) Cardiovasc. Drugs Ther., 5(Suppl 2),277‒287.
7) Vaziri, N.D. & Rodriguez-Iturbe, B. (2006) Nat. Clin. Pract.Nephrol., 2, 582‒593.
8) Bagul, P.K. & Banerjee, S.K. (2013) Curr. Pharm. Des., 19,5663‒5677.
9) Droge, W. (2002) Physiol. Rev., 82, 47‒95.
10) Halliwell, B. & Gutteridge, J.M. (1992) FEBS Lett.,307, 108‒112.
11) Radi, R. (2013) J. Biol. Chem., 288, 26464‒26472.
12) Lipinski, B. (2011) Oxid. Med. Cell. Longev., 2011, 809696.
13) Brewer, A.C., Mustafi, S.B., Murray, T.V.,Rajasekaran, N.S., &Benjamin, I.J. (2013) Antioxid. Redox Signal., 18, 1114‒1127.
14) Finkel, T. (1998) Curr. Opin. Biol, 10, 248‒253.
15) Liu, H., Colavitti, R., Rovira, I.I., & Finkel,T. (2005) Circ. Res.,97, 967‒974.
16) Endo, J., Sano, M., Katayama, T., Hishiki, T.,Shinmura, K.,Morizane, S., Matsuhashi, T., Katsumata, Y., Zhang, Y., Ito,H.,Nagahata, Y., Marchitti, S., Nishimaki, K., Wolf, A.M., Nakanishi,H.,Hattori, F., Vasiliou, V., Adachi, T., Ohsawa, I., Taguchi,R., Hirabayashi, Y.,Ohta, S., Suematsu, M., Ogawa, S., &Fukuda, K. (2009) Circ. Res.,105, 1118‒1127.
17) Ristow, M. & Zarse, K. (2010) Exp. Gerontol., 45, 410‒418.
18) Gan, L. & Johnson, J.A. (2014) Biochim. Biophys. Acta, 1842,1208‒1218.
19) Sauer, H., Wartenberg, M., & Hescheler, J. (2001)Cell.Physiol.Biochem., 11,173‒186.
20) Zhou, R., Yazdi, A.S., Menu, P., & Tschopp, J.(2011) Nature,469, 221‒225.
21) Garg, A.D., Dudek, A.M., Ferreira, G.B., Verfaillie,T., Vandenabeele,P., Krysko, D.V., Mathieu, C., & Agostinis, P. (2013)Autophagy,9, 1292‒1307.
22) Mates, J.M., Segura, J.A., Alonso, F.J., &Marquez, J. (2012)Arch. Toxicol.,86, 1649‒1665.
23) Steinhubl, S.R. (2008) Am. J. Cardiol., 101(10A),14D‒19D.
24) Bjelakovic, G., Nikolova, D., Gluud, L.L., Simonetti,R.G., &Gluud, C. (2007) JAMA, 297,842‒857.
25) Brambilla, D., Mancuso, C., Scuderi, M.R., Bosco, P.,Cantarella,G., Lempereur, L., Di Benedetto, G., Pezzino, S., &Bernardini,R. (2008) Nutr. J., 7,29.
26) Hackam, D.G.(2007) ACP J. Club, 147, 4.
27) Setsukinai,K., Urano, Y., Kakinuma, K., Majima, H.J., & Nagano,T. (2003) J. Biol. Chem., 278, 3170‒3175.
28) Motterlini, R.& Otterbein, L.E. (2010) Nat.Rev. Drug Discov., 9,728‒743.
29) Kimura, H.(2010) Antioxid.Redox Signal., 12, 1111‒1123.
30) Kajimura, M.,Fukuda, R., Bateman, R.M., Yamamoto, T., &Suematsu, M. (2010) Antioxid. Redox Signal., 13, 157‒192.
31) Kashfi, K.& Olson, K.R. (2013) Biochem.Pharmacol., 85, 689‒703.
32) Abraini, J.H.,Gardette-Chauffour, M.C., Martinez, E., 活性氧tain,J.C., & Lemaire, C. (1994) J. Appl. Physiol., 76, 1113‒1118.
33) Fontanari, P.,Badier, M., Guillot, C., Tomei, C., Burnet, H.,Gardette, B., & Jammes, Y.(2000) Eur. J.Appl. Physiol., 81,325‒328.
34) Hayashida, K.,Sano, M., Ohsawa, I., Shinmura, K., Tamaki, K.,Kimura, K., Endo, J., Katayama,T., Kawamura, A., Kohsaka, S.,Makino, S., Ohta, S., Ogawa, S., & Fukuda, K.(2008) Biochem.Biophys.Res. Commun., 373, 30‒35.
35) Ono, H.,Nishijima, Y., Adachi, N., Sakamoto, M., Kudo, Y.,Kaneko, K., Nakao, A., &Imaoka, T. (2012) Med. GasRes, 2, 21.
36) Ohsawa, I.,Nishimaki, K., Yamagata, K., Ishikawa, M., & Ohta,S. (2008) Biochem. Biophys. Res. Commun., 377, 1195‒1198.
37) Nagata, K.,Nakashima-Kamimura, N., Mikami, T., Ohsawa, I.,& Ohta, S. (2009) Neuropsychopharm, 34, 501‒508.
38) Kamimura, N.,Nishimaki, K., Ohsawa, I., & Ohta, S. (2011)Obesity (Silver Spring), 19, 1396‒1403.
39) Cai, J., Kang,Z., Liu, K., Liu, W., Li, R., Zhang, J.H., Luo, X., &Sun, X. (2009) Brain Res., 1256, 129‒137.
40) Nagatani, K.,Nawashiro, H., Takeuchi, S., Tomura, S., Otani, N.,Osada, H., Wada, K., Katoh,H., Tsuzuki, N., & Mori, K. (2013)Med. Gas Res, 3, 13.
41) Oharazawa, H.,Igarashi, T., Yokota, T., Fujii, H., Suzuki, H.,Machide, M., Takahashi, H.,Ohta, S., & Ohsawa, I. (2010)Invest. Ophthalmol. Vis. Sci., 51, 487‒492.
42) Kubota, M.,Shimmura, S., Kubota, S., Miyashita, H., Kato, N.,Noda, K., Ozawa, Y., Usui,T., Ishida, S., Umezawa, K., Kurihara,T., & Tsubota, K. (2011) Invest. Ophthalmol. Vis. Sci., 52,427‒433.
43) Noda, K.,Shigemura, N., Tanaka, Y., Kawamura, T., Hyun Lim,
S., Kokubo, K.,Billiar, T.R., Bermudez, C.A., Kobayashi, H., &Nakao, A. (2013) J. Heart Lung Transplant., 32, 241‒250.
44)Nakashima-Kamimura, N., Mori, T., Ohsawa, I., Asoh, S., &Ohta, S. (2009) Cancer Chemother. Pharmacol., 64, 753‒761.
45) Shimouchi, A.,Nose, K., Shirai, M., & Kondo, T. (2012) Adv.Exp. Med. Biol., 737, 245‒250.
46) Wang, F., Yu,G., Liu, S.Y., Li, J.B., Wang, J.F., Bo, L.L., Qian,L.R., Sun, X.J., &Deng, X.M. (2011) J. Surg.Res., 167, e339‒e344.
47) Hayashida, K.,Sano, M., Kamimura, N., Yokota, T., Suzuki, M.,Maekawa, Y., Kawamura, A., Abe,T., Ohta, S., Fukuda, K., &Hori, S. (2012) J. Am. Heart Assoc, 1, e003459.
48) Buchholz,B.M., Kaczorowski, D.J., Sugimoto, R., Yang, R.,Wang, Y., Billiar, T.R.,McCurry, K.R., Bauer, A.J., & Nakao, A.(2008) Am. J. Transplant., 8, 2015‒2024.
49) Cardinal,J.S., Zhan, J., Wang, Y., Sugimoto, R., Tsung, A., Mc-Curry, K.R., Billiar,T.R., & Nakao, A. (2010) KidneyInt., 77,101‒109.
50) Fukuda, K.,Asoh, S., Ishikawa, M., Yamamoto, Y., Ohsawa, I.,& Ohta, S. (2007) Biochem. Biophys. Res. Commun., 361, 670‒674.
51) Federico, A.,Cardaioli, E., Da Pozzo, P., Formichi, P., Gallus, G.N., & Radi, E. (2012) J. Neurol. Sci., 322, 254‒262.
52) Liu, J., Wang,X., Shigenaga, M.K., Yeo, H.C., Mori, A., &Ames, B.N. (1996) FASEB J., 10, 1532‒1538.
53) Becker, S.& Wojtowicz, J.M. (2007) TrendsCogn. Sci., 11, 70‒76.
54) Schapira, A.H.(2008) LancetNeurol., 7, 97‒109.
55) Fu, Y., Ito,M., Fujita, Y., Ichihara, M., Masuda, A., Suzuki, Y.,Maesawa, S., Kajita, Y.,Hirayama, M., Ohsawa, I., Ohta, S., &Ohno, K. (2009) Neu活性氧ci.Lett., 453, 81‒85.
56) Fujita, K.,Seike, T., Yutsudo, N., Ohno, M., Yamada, H., Yamaguchi,H., Sakumi, K.,Yamakawa, Y., Kido, M.A., Takaki, A.,Katafuchi, T., Tanaka, Y., Nakabeppu, Y.,& Noda, M. (2009)PLoS ONE, 4, e7247.
57) Yoritaka, A.,Takanashi, M., Hirayama, M., Nakahara, T., Ohta,S., & Hattori, N. (2013) Mov. Disord., 28, 836‒839.
58) Song, G., Li,M., Sang, H., Zhang, L., Li, X., Yao, S., Yu, Y.,Zong, C., Xue, Y., & Qin,S. (2013) J. LipidRes., 54, 1884‒1893.
59) Aoki, K.,Nakao, A., Adachi, T., Matsui, Y., & Miyakawa, S.(2012) Med. Gas Res, 2, 12.
60) Ishibashi, T.,Sato, B., Shibata, S., Sakai, T., Hara, Y., Naritomi,Y., Koyanagi, S., Hara,H., & Nagao, T. (2014) Int.Immunopharmacol.,21, 468‒473.
61) Kang, K.M.,Kang, Y.N., Choi, I.B., Gu, Y., Kawamura, T.,Toyoda, Y., & Nakao, A. (2011)Med. Gas Res, 1, 11.
62) Chuai, Y.,Gao, F., Li, B., Zhao, L., Qian, L., Cao, F., Wang, L.,Sun, X., Cui, J., &Cai, J. (2012) Biochem.J., 442, 49‒56.
63) Niki, E.(2014) Biochim.Biophys. Acta, 1840, 809‒817.
64) Shinbo, T.,Kokubo, K., Sato, Y., Hagiri, S., Hataishi, R., Hi活性氧e, M., &Kobayashi, H. (2013) Am. J.Physiol. Heart Circ. Physiol.,305, H542‒H550.
65) Zhang, Y.,Sun, Q., He, B., Xiao, J., Wang, Z., & Sun, X. (2011)Int. J. Cardiol., 148, 91‒95.
66) Itoh, T.,Fujita, Y., Ito, M., Masuda, A., Ohno, K., Ichihara, M.,Kojima, T., Nozawa, Y.,& Ito, M. (2009) Biochem.Biophys. Res.Commun., 389, 651‒656.
67) Chen, H., Sun,Y.P., Li, Y., Liu, W.W., Xiang, H.G., Fan, L.Y.,Sun, Q., Xu, X.Y., Cai, J.M.,Ruan, C.P., Su, N., Yan, R.L., Sun,X.J., & Wang, Q. (2010) Biochem. Biophys. Res. Commun., 393,308‒313.
68) Kawamura, T.,Wakabayashi, N., Shigemura, N., Huang, C.S.,Masutani, K., Tanaka, Y., Noda, K.,Peng, X., Takahashi, T., Billiar,T.R., Okumura, M., Toyoda, Y., Kensler, T.W.,& Nakao, A.(2013) Am. J.Physiol. Lung Cell. Mol. Physiol., 304, L646‒L656.
69) Matsumoto, A.,Yamafuji, M., Tachibana, T., Nakabeppu, Y.,Noda, M., & Nakaya, H. (2013) Sci. Rep, 3, 3273.
70) Terasaki, Y.,Ohsawa, I., Terasaki, M., Takahashi, M., Kunugi,S., Dedong, K., Urushiyama, H.,Amenomori, S., Kaneko-Togashi, M., Kuwahara, N., Ishikawa, A., Kamimura, N.,Ohta,S., & Fukuda, Y. (2011) Am. J. Physiol. Lung Cell. Mol. Physiol.,301, L415‒L426.
71) Wood, K.C.& Gladwin, M.T. (2007) Nat.Med., 13, 673‒674.
72) Ito, M.,Hirayama, M., Yamai, K., Goto, S., Ito, M., Ichihara, M.,& Ohno, K. (2012) Med. Gas Res, 2, 15.
73) Zeng, J.,Zhang, M., & Sun, X. (2013) PLoS ONE, 8, e71038.
74) Lin, Y.,Zhang, W., Qi, F., Cui, W., Xie, Y., & Shen, W. (2014)J. Plant Physiol., 171, 1‒8.
作者素描

●太田 成男(おおた しげお)
日本医科大学院医学研究科生物学领域教授.
■简历:1951年出生于福岛县.74年毕业于东京大学理学部,79年毕业于东京大学大学院药学系研究科博士课程,81年毕业于瑞士联邦巴塞尔大学生物中心研究所研究员,85年自治医科大学生化学教室讲师,91年同副教授,94年开始现职.
■研究主题和抱负:主题是氢医学、线粒体医学.虽然氢还存在许多尚未明白的问题但同时也有无限的可能性,为了让任何人都能理解,希望尽力详细地阐明分子机构。另外,为了让氢作为医药得到认可,希望能提供临床试验上的帮助。







